Л.И. Егоренков, Б.И. Кочуров
Геоэкология
Учебное пособие. – М.: Финансы и статистика, 2005. — 320 с.
| Предыдущая |
Содержание статьи:
Глава 2. Антропогенное преобразование ландшафтов (геосистем)
2.7. Миграция отдельных загрязнителей в биокосных системах
2.7.3. Тяжелые металлы в окружающей среде
В результате промышленных и производственных процессов во внешнюю среду выбрасывается большое количество отходов, содержащих различные соединения тяжелых металлов (ТМ), которые являются токсичными для растений, животных и человека. Особую опасность представляет загрязнение биосферы такими металлами, как ртуть, мышьяк, кадмий и свинец. Значительное поступление некоторых ТМ в окружающую среду происходит при использовании их соединений в качестве ядохимикатов — пестицидов и удобрений. Большую тревогу в настоящее время вызывают огромные накопления осадков сточных вод (промышленных, бытовых и сельскохозяйственных), которые содержат много органических веществ, азота, фосфора и калия и могли бы считаться ценными органическими удобрениями.
Однако наличие в них большого количества ТМ делает проблематичным их применение в сельском хозяйстве, а имеющийся зарубежный опыт указывает на необходимость большой осторожности при их использовании в растениеводстве.
При антропогенном загрязнении окружающей среды ТМ накапливаются в почве чаще всего не отдельно, а совместно. Это приводит к тому, что накапливающиеся в ней избыточные ТМ начинают поступать в растения, а через них в организм животных и человека.
Для оценки масштаба загрязнения почв тяжелыми металлами важно знать их естественное фоновое содержание (табл. 2.7).
Тяжелые металлы накапливаются в почвах в разной форме — в виде ионов в почвенном растворе они входят в состав органно-минеральных комплексов, адсорбируясь на поверхности коллоидных частиц.
В окислительных условиях при снижении рН растворимость металлов увеличивается, а в восстановительных, наоборот, уменьшается.
Таблица 2.7. Концентрации различных элементов в почве (предельно допустимые для растений, мг/кг)
|
Элемент |
Естественное фоновое содержание |
Предельно допустимая концентрация |
|
Be |
0,1-10 |
10 |
|
F |
10-500 |
500 |
|
В |
2-100 |
100 |
|
Cr |
1-100 |
100 |
|
Ni |
1-100 |
100 |
|
Co |
1-50 |
50 |
|
Cu |
2-100 |
100 |
|
Zn |
10-300 |
300 |
|
As |
1-50 |
50 |
|
Se |
0,1 -100 |
10 |
|
Mo |
0,2-10 |
10 |
|
Cd |
0,01 -1 |
5 |
|
Hg |
0,01 -1 |
5 |
|
Pb |
0,1-10 |
100 |
Тяжелые металлы проникают в растение в основном через корневую систему, причем элементы, которые входят в состав жизненно важных соединений, поглощаются из почвы растениями избирательно.
По способности накапливать тяжелые металлы ткани основных органов растений можно расположить в следующем порядке: корни, листья, семена (плоды).
Растения обладают способностью в случае очень сильного загрязнения почвы усиливать формирование главного защитного организма — корневой системы за счет сокращения биомассы надземной части. Эту реакцию растительного организма следует рассматривать как вынужденную потребность растения усилить емкость корней.
Поступая в биосферу, ТМ активно включаются в миграционные циклы, аккумулируются в различных компонентах экосистем, в том числе в гидробионтах. Тяжелые металлы представляют чрезвычайную опасность как загрязнители природных вод. Ионы ТМ сохраняются в природных водах постоянно при любых условиях. Кроме того, тяжелые металлы даже в сравнительно малых концентрациях могут оказывать токсическое воздействие на водные организмы. Среди ТМ первое место по растворимости и токсичности занимает ртуть. Антропогенное загрязнение водных систем добавляет к естественному выносу тяжелых металлов из горных пород двукратное количество ртути и 12-13-кратное количество свинца, меди, цинка.
Одним из важных последствий действия тяжелых металлов на водные экосистемы является изменение структуры планктона и бентоса.
Многочисленными исследованиями на Белом и Балтийском морях установлено воздействие ТМ на изменение состава, численности и биомассы фитопланктона, на смену доминирующих видов. Эти данные о перестройке водных сообществ под действием ТМ имеют большое практическое значение. Токсическое действие на отдельных представителей фитопланктона и фитобентоса в конечном итоге оказывает большое влияние на продуктивность водных сообществ в целом, а также на качество воды, пригодность которой для различных видов водопользования определяется во многом нормальным функционированием гидро-бионтов. В связи с процессами накопления ТМ по трофической цели адаптивные явления несут угрозу существованию не только для видов гидробионтов, но в итоге и для человека.
Ядовитое действие ионов тяжелых металлов в значительной мере связано с их способностью прочно соединяться с белками и нарушать нормальную работу ферментов и других биологически активных белковых веществ.
Когда речь идет о ядовитости самого металла, то, как правило, он проявляет токсический эффект в тонкоизмельченном состоянии (в виде пылевых частиц). Попадая в легкие и бронхи, частицы металла вызывают раздражение и, медленно реагируя с клеточным содержимым, превращаются в соединения, которые переходят в кровь. Аналогичное действие оказывает и вдыхание пылевых частиц оксидов металлов или их солей. Соли некоторых металлов сильно раздражают кожу (например, соли магния) и способны всасываться даже через кожные покровы.
Опасными, т. е. действующими даже в малых концентрациях, следует считать также свинец, кадмий, таллий, бериллий, хром, барий, стронций. Несколько менее опасны марганец, литий, никель, цинк.
Ртуть. Среднее содержание ртути в земной коре равно 0,08 мг/кг, в почвах 0,04-0,8 мг/кг, в растительных продуктах 0,001-0,64 мг/кг.
Пары ртути задерживаются в легких и могут всасываться в кишечнике, что, по-видимому, связано с относительно хорошей растворимостью металлической ртути в воде. Ионы ртути (как и других тяжелых металлов) энергично соединяются с группами SH белков и прочно удерживаются в получившихся комплексах. При этом ртуть в тканях организма частично переходит в сульфид. Белки, богатые вышеназванными группами, содержатся в почках, поэтому ртуть, попадая в организм, сосредоточивается преимущественно в почках, нарушая их нормальную деятельность, а также в клетках мозга и слизистой оболочке рта.
Следует избегать контактов с металлической ртутью. Даже если, например, в комнате разбился медицинский термометр, следует учитывать опасность отравления парами ртути, потому что ее предельно допустимая доза очень мала — 0,00001 мг/л. Раскатившиеся шарики ртути бывает трудно собрать; в этом случае лучше засыпать место, где могут оказаться мелкие частицы ртути, порошком серы или залить раствором хлорида железа. Поверхность ртути при этом будет окислена и испарение резко уменьшится.
В России существуют жесткие требования к содержанию ртути в продуктах: допустимая остаточная концентрация (ДОК) элемента в хлебо- и зернопродуктах равна 0,01, в овощах — 0,02, во фруктах — 0,01 мг/кг сырого веса.
Для уменьшения потока ртути из почвы в растения необходимо повысить рН среды. При известковании почвы в растения поступает ртути почти в 2 раза меньше.
В природной циркуляции ртути важную роль играют водоемы. Накапливаясь в грунте и донных отложениях, ртуть и ее соединения в течение длительного времени диффундируют в воду. Концентрация ртути увеличивается почти на порядок в каждом последующем звене пищевой цепи.
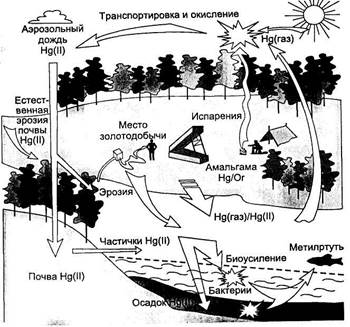
Показательны в этом отношении исследования во Французской Гвиане, которые были обобщены и опубликованы в 2002 г. французскими профессорами Л. Шарле (ун-т Гренобля) и А. Буду (ун-т Бордо). В 1994 г. сотрудниками Национального центра исследований общественного здоровья в Инсерме было обнаружено заражение ртутью индейцев племени вайа-нас, проживающих в отдаленных районах Гвианы. Дальнейшие исследования, которые проводились здесь многими научными коллективами, начиная с 1998 г., подтвердили причастность к этим явлениям старателей золотых приисков. Современные старатели, в основном нелегалы, работают на старых приисках и используют элементарную ртуть для добычи золота. Прежде всего они уничтожают зеленый покров и поверхность почвы, затем размывают почву водой, заливая ее в ямы добычи.
Всплывающие осадки всасываются мощными насосами, выбрасывая их на наклонные столы, которые удерживают золотые песчинки. Ртуть — единственный жидкий металл, который при обычной температуре воздуха способен концентрировать мельчайшие частички золота, превращая их в амальгаму, похожую на ту, что применяется для пломбирования зубов. Во время этого процесса часть ртути попадает в реку в форме жидких шариков, как из разбитого термометра. Амальгама подогревается, ртуть испаряется, золото выпадает в осадок.
В среднем на каждый килограмм добытого золота расходуется 1,3 кг элементарной ртути, от 65 до 85% которой испаряется в атмосферу. Так от 5 до 10 т ртути в год выбрасывается в атмосферу, почву и реки Гвианы.
Ртуть существует в трех основных формах: элементарная ртуть (Hg), двухвалентная ртуть [(Hg(II)] и метилртуть, которая является наиболее токсичной формой ртути для человека.
В местных почвах содержание ртути в 3-х метровой толще составляет в среднем около 1000 мг/м2. Ртуть в почве малоподвижна, большая ее часть прочно связана с органическими соединениями. Причем более 90% ртути остается в почве и после 20-летнего периода. Однако любые процессы, вызывающие эрозию почвы (дожди, наводнения, уничтожение лесов, рытье шахт, строительство дорог и т.д.), значительно усиливают приток воды, а следовательно, и ртути. Она попадает в поверхностные и подземные воды (рис.2.13).
В водной аэробной среде содержание метилртути обычно не превышают 1% общего содержания ртути в воде. В водной среде, лишенной кислорода (в анаэробных условиях) происходит процесс трансформации двухвалентной ртути, который называется метиляцией.
Этот процесс осуществляется при помощи бактерий, связанных с серным циклом (сульфатоограничивающие бактерии). Некоторые бактерии способны разложить в свою очередь и метилртуть, превращая ее в элементарную ртуть.
Благоприятные условия для образования метилртути создаются обычно на глубинах более 5 м в ряде водохранилищ на границах плотин и в болотах. Таким образом, водохранилища являются своеобразными биореакторами для превращения ртути в метилртуть.
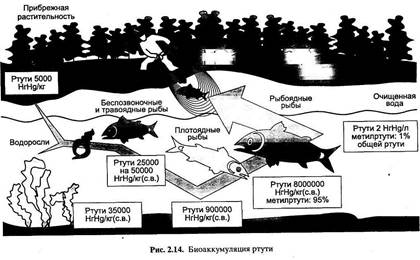
Несмотря на незначительное содержание метилртути в воде, она в процессе биоаккумуляции может достичь внушительных концентраций в мускульной ткани наиболее ценных пород рыб (рис.2.14).
На этом рисунке концентрация ртути показана в нанограммах (тысячная доля грамма) на 1 л воды. Причем в хищных рыбах содержится в 1000 раз больше ртути, чем в травоядных. В свою очередь, концентрация ртути в мышцах хищных рыб в сотни раз превышает ее содержание в водных и наземных растениях и в 4 млн раз — ее концентрацию в воде (рис. 2.14).
Употребляя в пищу некоторые породы хищных (ценных) рыб, индейцы заражаются метилртутью, которая накапливается преимущественно в волосах. Содержание ртути в волосах превышает ее концентрацию в крови почти в 250 раз. У 57% населения племени вайонас, о котором говорилось выше, содержание ртути в волосах превышало норму, рекомендуемую ВОЗ (Всемирной организацией здравоохранения), которая составляет 10 Нг/г.
Население в возрасте от 15 до 45 лет потребляет здесь в среднем 350 г рыбы в день. Уровень заражения рыбы таков, что количество ртути, потребляемой с рыбой в неделю, колеблется от 200 до 450 Нг, что в 2 раза превышает еженедельную норму потребления, рекомендованную ВОЗ.
Результатом потребления ртути, содержащейся в рыбе, явились значительные отклонения от нормы у детей — нарушение координации движения ног, ограничение зрительного обзора-
В большей степени подвержены риску сами старатели. Во время нагрева амальгамы они непосредственно испытывают воздействие выделяемых паров ртути. Это выражается в обострении хронических заболеваний, нарушении дыхания, дисфункции центральной нервной системы (трясущиеся руки, нервный тик лица, спазм губ и др.), нарушение деятельности почек и желудка.
Проблема загрязнения ртутью неизбежно требует решения экономических, социальных, культурных и политических проблем, связанных с добычей золота.
Свинец. Из числа соединений свинца наибольший интерес представляют карбонаты и хроматы свинца, используемые как неорганические пигменты (краски), а также различные оксиды и сульфат, которыми заправляются аккумуляторы. В 1853 г. немецкий химик К. Левич получил тетраэтилсвинец, ядовитую жидкость высокой плотности. А в 1921 г. американцы Миджлей и Байд, добавляя этот яд в бензин, снизили его детонацию и повысили кпд автомобильных двигателей.
С тех пор при использовании каждого литра этилированного бензина в окружающую среду выбрасывается около 400 мг свинца. Теперь городской воздух в 20 раз грязнее загородного и в 2 тысячи раз богаче свинцом, чем морской.
Опасная для человека концентрация равна восьми частям свинца на 10 миллионов частей крови. Предельное содержание в соках, фруктах, консервах — 0,5 мг на тонну.
Отравление соединениями свинца чаще всего носит хронический характер.
Обычно оно развивается при вдыхании пыли, содержащей свинец или его соединения, в условиях недостаточного соблюдения правил техники безопасности. Свинец удерживается белками эритроцитов, затем поступает в плазму крови (в виде комплексов с гамма-глобулином) и, наконец, достигает почек, печени и других органов. В костях свинец накапливается постепенно и долго остается там. Время от времени происходит выделение свинца из костей, что может стать причиной неожиданного развития симптомов острого отравления. Долгое время свинец остается и в головном мозге. Кроме того, поражение десен, расстройство кишечника, заболевание почек и нервной системы являются результатом отравления свинцом.
Кадмий. Концентрация кадмия в основных типах почв России равна 0,01-0,04. Помимо других основных источников загрязнения, он попадает на сельскохозяйственные земли с удобрениями в виде шламов сточных вод, с фосфорными удобрениями и гербицидами.
При внесении в почву соединений элемента в дозах от 1 до 10 мг/кг подавляющее его количество задерживается в верхнем пахотном горизонте (0-20 см). Некоторое количество кадмия может мигрировать вглубь почвы в условиях промывного режима.
Считается, что кадмий достаточно легко проникает из почвы в надземную часть растений, однако в опытах с питательными растворами основная часть элемента задерживалась в корнях. Кадмий проникает в растения преимущественно в фазу кущения, а в период колошения его количество в вегетативных частях резко уменьшается.
Однако те количества кадмия, которые не приносят вреда растениям, могут оказать пагубное влияние на здоровье человека, поскольку этот металл обладает высокими кумулятивными способностями. Из животного организма кадмий удаляется чрезвычайно медленно — в течение 20—40 лет.
Ядовиты как сам кадмий, так и его соединения. Ионы этого металла вступают в соединение с карбоксильными, аминными и сульфгидроксильными (-ССОН, -NH2, -SH) группами, имеющимися в молекулах белков, и таким путем задерживаются в организме. Кадмий годами может оставаться в таких органах, как почки, печень, поджелудочная железа, щитовидная железа. Действуя на кожу, кадмий вызывает дерматиты и экземы.
Мышьяк относится к тяжелым металлам, но поскольку антропогенное загрязнение биосферы этим элементом довольно существенно, то представляется целесообразным рассмотреть поведение этого токсического элемента в почвах и Растениях.
Среднее содержание мышьяка в земной коре равно 3,4 мг/кг. Содержание мышьяка в почвах мира в среднем составляет 5-6 мг/кг.
По особенностям гипергенной миграции мышьяк следует отнести к слабоподвижным аниогенным элементам. Он более подвижен в окислительной и менее подвижен в восстановительной сероводородной обстановках.
В небольших количествах мышьяк всегда присутствует в растениях. Содержание мышьяка в основных сельскохозяйственных культурах, выращенных на незагрязненных почвах, сравнительно невелико (0,03-4,2 мг/кг сухой массы).
Различные сельскохозяйственные культуры проявляют неодинаковую толерантность к избытку мышьяка в почве. Толерантными считаются рожь, пшеница, овес, картофель, томаты, морковь, однолетние злаковые травы; умеренно толерантными — кукуруза, свекла, кабачки; малотолерантными — горох, фасоль, соя, рис, огурцы.
Значительное количество мышьяка поступает в почву при применении мышьякосодержащих пестицидов, в том числе инсектофунгицидов.
Неорганические препараты мышьяка, используемые в сельском хозяйстве, мало летучи и могут долго сохраняться в почве.
Значительно меньшим загрязнителем почвы являются минеральные удобрения. По некоторым данным с азотными удобрениями в почву поступает 1-10 г/га мышьяка, а с суперфосфатом — 30 — 300 мг/кг.
Для снижения токсического действия мышьяка на растения и уменьшения его потока в пищевой цепи предлагаются различные приемы, например внесение в почву некоторых минеральных удобрений — фосфата натрия, сульфата аммония, хлористого калия, обладающих эллюационной способностью, которые обеспечивают вытеснение мышьяка из почвенного поглощающего комплекса и способствуют его вымыванию.
Содержание мышьяка в растительной продукции жестко нормируется. Так, Министерством здравоохранения СССР еще в 1981 г. было утверждено допустимое количество элемента в хлебо- и зернопродуктах, овощах, фруктах равное 0,2 мг/кг сырой массы.
| Предыдущая |
