Ю.А. Александров
Основы радиационной экологии
Учебное пособие. – Йошкар-Ола: Мар. гос. ун-т, 2007. – 268 с.
| Предыдущая |
Содержание статьи:
Раздел 3. Биологическое действие ионизирующих излучений
3.5. Действие ионизирующих излучений на критические системы организма
3.5.1. Основные механизмы гемо- и иммунопоэза
Костный мозг – типичный образец системы клеточного обновления, обеспечивающей поддержание постоянства числа клеток с ограниченным периодом жизни, в данном случае – клеток крови. В костном мозге, как и в других органах гемопоэза, различают собственно кроветворные клетки и стромальные элементы, создающие необходимое микроокружение для размножения и развития кроветворных клеток.
В соответствии с признаваемой большинством исследователей унитарной моделью кроветворения родоначальными для всех ростков гемопоэза являются полипотентные стволовые кроветворные клетки. Отличительной их чертой является то, что стволовые клетки способны делиться неограниченное число раз, воспроизводя себе подобных. Часть же потомков стволовых клеток коммитируется, то есть приобретает способность к дифференцировке в направлении ограниченного числа ростков или даже какого-то одного определенного ростка кроветворения. Пролиферативная активность и способность к самоподдержанию коммитированных стволовых клеток ограничены. Под терминами «стволовой пул» и «стволовой отдел» кроветворной системы понимают совокупность полипотентных и коммитированных стволовых кроветворных клеток (СКК).
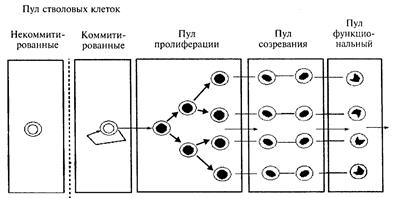
Рис. 10. Схема функционирования систем клеточного обновления
(по Т. Флиднеру, 1974)
Считается, что у человека около 0,3-0,7% клеток костного мозга относятся к стволовому пулу. Причем в норме около 90% стволовых клеток находятся в стадии покоя (Go-стадия) клеточного цикла.
Пройдя ряд делений – стадий созревания, клетки полностью утрачивают свойства стволовых и дают начало уже морфологически распознаваемым клеткам-предшественникам. Последние способны совершить еще несколько делений (обычно 4-5), одновременно созревая, и составляют так называемый пролиферативно-созревающий (делящийся-созревающий) пул или отдел. В миелоидном ряду в состав этого пула входят миелобласты, промиелоциты, миелоциты; в эритроидном – эритробласты, пронормоциты, базофильные и полихроматофильные нормоциты и т.д.
Утратив способность к пролиферации, кроветворные клетки продолжают дифференцировку уже без деления и формируют созревающий пул. В миелоидном ряду – это метамиелоциты, отчасти палочкоядерные гранулоциты; в эритроидном – оксифильные нормоциты, ретикулоциты. И лишь завершив созревание, клетки выходят в циркуляцию, образуя функциональный пул: сегментоядерные гранулоциты, моноциты, эритроциты, пластинки (отшнуровавшиеся участки цитоплазмы мегакариоцитов). Предшественники лимфоцитов также образуются из полипотентной стволовой кроветворной клетки в костном мозге. В-лимфоциты дозревают здесь же, а предшественники Т-лимфоцитов мигрируют в вилочковую железу, где после прохождения иммунологического отбора (гибели клеток, реагирующих на аутоантигены) оставшиеся клетки дозревают в корковом веществе. Зрелые Т- и В-лимфоциты поступают в периферическую кровь и многократно мигрируют через вторичные лимфоидные органы (лимфатические узлы, селезенку, миндалины, пейеровы бляшки). Под влиянием антигенных стимулов происходит дифференцировка чувствительных к этим антигенам лимфоцитов, их последующая пролиферация на территориях вторичных лимфоидных органов и созревание (В-лимфоциты частично превращаются в плазматические клетки).
Полагают, что у человека время прохождения гранулоцитов через пролиферативно-созревающий пул составляет 4-6 сут. и примерно столько же времени требуется для прохождения через пул созревания. Эритроциты развиваются в костном мозге в течение 7-8 сут., тромбоциты – 5-7 сут., а моноциты созревают за 55-60 часов. В периферической крови зрелые гранулоциты сохраняются в среднем 8-10 ч, после чего мигрируют в ткани, где существуют еще 1-2 суток. Период жизни в крови эритроцитов составляет 100-120 сут., тромбоцитов – 8-10 сут., а моноциты находятся в функциональном пуле около 30-60 ч (по некоторым данным 12-20 ч), после чего мигрируют в ткани, где трансформируются в макрофаги. Продолжительность жизни лимфоцитов может составлять от нескольких суток до многих десятков лет.
Ежедневно кроветворной тканью человека производится около 12×1010 гранулоцитов, 15×1010 тромбоцитов, 2×1010 лимфоцитов, 24×1010 эритроцитов.
Клетки крови осуществляют в организме многие жизненно важные функции.
ГРАНУЛОЦИТЫ (в основном нейтрофилы, но также и эозинофилы, ба-зофилы) содержат многочисленные мембранные структуры и богаты лизосомами. Гранулы нейтрофилов и эозинофилов содержат в большом количестве бактерицидные вещества. В гранулах базофилов содержатся гепарин и вазоактивные амины. Благодаря способности к хемотаксису и особым рецепторным свойствам гранулоциты быстро и в большом количестве накапливаются в воспалительных очагах, выполняя там свои основные функции: биоцидную (внеклеточный киллинг и фагоцитоз микроорганизмов), цитотоксическую (участие в механизмах противоопухолевого иммунитета) и регуляторную (регуляция процессов воспаления, регенерации тканей и т.п.).
МОНОЦИТЫ, проникая из крови в соединительную ткань, особенно в таких органах, как печень, селезенка, костный мозг, легкие, трансформируются в макрофаги. Тканевые макрофаги вместе с циркулирующими в крови моноцитами формируют так называемую систему мононуклеарных фагоцитов или, по-старому, ретикулоэндотелиальную систему. Клетки этой системы активно фагоцитируют микробы, вирусные частицы, продукты распада клеток, старые эритроциты и другие антигенные материалы, подготавливают антигены для распознавания их лимфоцитами, синтезируют и секретируют ряд медиаторов иммунного ответа (интерферон, лизоцим, простагландины и т.п.) и другие биологически активные вещества. Клетки системы мононуклеарных фагоцитов активно вырабатывают интерлейкин-1 (цитокин), как непосредственно влияющий на пролиферацию и дифференцировку кроветворных клеток, так и стимулируюший размножение фибробластов и выработку последними колониестимулирующих факторов и ряд других цитокинов.
ТРОМБОЦИТЫ (кровяные пластинки) представляют собой фрагменты цитоплазмы мегакариоцитов. Они играют важнейшую роль в процессе свертывания крови, непосредственно участвуя в образовании кровяного тромбопластина, ретракции кровяного сгустка и выполняя другие функции. Кроме того, они обладают ангиотрофической или эндотелий поддерживающей функцией, способствуют сохранению нормальной структуры сосудистой стенки, ее резистентности и непроницаемости для эритроцитов. Краевое стояние тромбоцитов обеспечивает прикрытие межэндотелиальных щелей в стенках капилляров, а фрагменты тромбоцитов включаются в цитоплазму эндотелиальных клеток, обеспечивая снабжение последних необходимыми субстратами. Тромбоциты также образуют «пробки» у мест повреждения сосудистого эндотелия и транспортируют туда необходимые для свертывания факторы. Кроме того, тромбоциты принимают участие в воспалительной реакции, освобождая бактерицидные продукты.
ЛИМФОЦИТЫ являются важнейшими компонентами системы специфической защиты организма – иммунитета. Основной функцией В-лимфоцитов, как и их потомков – плазматических клеток, является участие в реакциях гуморального иммунитета: продукция и секреция иммуноглобулинов – специфических антител против различных антигенов.
Т-лимфоциты участвуют в осуществлении клеточного иммунитета путем непосредственного контакта с клетками-мишенями (реакции трансплантационного иммунитета, гиперчувствительности замедленного типа и др.). Кроме того, специализированные группы Т-лимфоцитов (супрессоры и хелперы) участвуют в осуществлении кооперативного взаимодействия клеток разного типа в реакциях как клеточного, так и гуморального иммунитета, стимулируя или, наоборот, подавляя эти реакции.
К группе Т-лимфоцитов относятся и клетки, влияющие на направление дифференцировки и процессы миграции стволовых клеток, на процесс послелучевого восстановления костномозгового кроветворения. Кроме того, Т-лимфоциты способны вырабатывать интерлейкин-3, важный регулятор пролиферативной активности стволовых кроветворных клеток.
ЕК-клетки (естественные клетки-киллеры) препятствуют возникновению злокачественных опухолей, вирусных и других инфекционных заболеваний. Они обладают способностью спонтанно, то есть без предварительной сенсибилизации антигеном, и без ограничений, связанных с молекулами главного комплекса гистосовместимости, убивать опухолевые, вирусинфицированные и другие виды анормальных клеток. Осуществляя иммунологический надзор, ЕК-клетки организуют «первую линию защиты» против роста опухолей, метастазов, развития лейкемии, вирусных и других инфекционных заболеваний в организме до того периода, пока в борьбу не вступят антигенспецифические факторы иммунитета.
Эритроциты являются переносчиками кислорода и углекислоты, обеспечивая тем самым тканевое дыхание. Они также выполняют важную роль в поддержании кислотно-щелочного баланса организма.
| Предыдущая |
